APUNTES TEORICOS
PLAN DEL PRIMER TRIMESTRE
Introducción a la quimica
A.Generalidades
A.1 La química a través de la historia
Definición de química y materia
La alquimia
La química de los siglos XVII y XIX
La química moderna
A.2.El trabajo científico
método científico y los recursos metodológicos
usados por los cientificos
Concepto de método y técnica
Paso del método científico
Aplicación del método científico
Las mediciones
concepto de medición
Tipos de medición
Unidades de medidas y sus conexiones
Potenciación y notación exponencial
B. Materia y energía
B.1 Propiedades de la materia
B.2 Clasificación de la materia
B.3 Separación de mezclas
B.4 La energia y la materia
-Tipo de energía
-Ley de lavoisier
-Transformaciones de la energía y de la materia
C .Estructura atómica
C.1 Concepto de átomo .concepto básicos
- El atómo a través del tiempo
-Algunas propiedades del átomo
C.2.Modelo atómico actual
-Antecedentes
-Modelo de bohr
-El modelo de sommerfield
-Hacia un modelo mecanico -cuántico de la materia
-Arquitectura electrónica
C.3 Diferencia entre átomo , elemento , compuesto y mezcla .
LA QUIMICA A TRAVÉS DE LA HISTORIA

Los primeros hombres que poblaron la Tierra tomaron los objetos de la naturaleza tal como los encontraban: la rama de un árbol como un garrote, una piedra como un proyectil, los frutos de los árboles para mitigar su hambre, etcétera.
Con el paso del tiempo, los hombres empezaron a transformar la naturaleza Primero aprendieron a tallar las piedras, dándoles un borde cortante y una forma que permitiera sujetarlas fácilmente. El siguiente paso consistió en unir la piedra a un trozo de madera. Pero la piedra seguía siendo piedra y la madera seguía siendo madera.
En ocasiones en la naturaleza ocurrían cambios muy rápidos. Un rayo podía incendiar un bosque y reducirlo a cenizas, la carne se descomponía y olía mal, y el jugo de las frutas podía agriarse con el tiempo, o convertirse en una bebida estimulante; estos cambios que sufría la materia alteraban su estructura fundamental; dicho en otras palabras, ocurría un cambio químico.
Una de las primeras reacciones químicas llevadas a cabo voluntariamente por el hombre ocurrió probablemente cuando fue capaz de producir y mantener el fuego, esto implicó que tuviera que secar la madera, reducir una parte a pequeñas porciones para facilitar su encendido y emplear algún método como el frotamiento para alcanzar el punto de ignición.
Posteriormente descubrió que el calor generado por el fuego producía alteraciones en los alimentos cambiando su color, textura y sabor; lo que hoy se conoce como cocción de los alimentos. Avanzando a tientas, el hombre fue adquiriendo paulatinamente conocimiento químicos. En ocasiones era gracias a la casualidad, pero principalmente fue la necesidad de elaborar los materiales y alimentos para satisfacer sus necesidades la que lo guió en este largo aprendizaje.
DEFINICION DE LA QUIMICA Y LA MATERIA
es la ciencia que estudia tanto la composición, estructura y propiedades de la materia como los cambios que ésta experimenta durante las reacciones quimicas y su relación con la energía
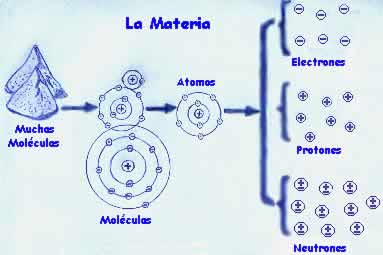
Componente principal de los cuerpos, susceptible de toda clase de formas y de sufrir cambios, que se caracteriza por un conjunto de propiedades físicas o químicas, perceptibles a través de los sentidos.
LA ALQUIMIA

Doctrina y estudio experimental de los fenómenos químicos que se desarrolló desde la Antigüedad y a lo largo de la época medieval y que pretendía descubrir los elementos constitutivos del universo, la transmutación de los metales, el elixir de la vida, etc.
SIGLO XVII

Los intentos prácticos de mejorar el refinado de las menas minerales y la extracción de los metales a partir de ellas fue una importante fuente de información para los químicos del siglo XVI. Entre ellos destaca Georgius Agricola (1494–1555), que publicó la gran obra De metalica (Sobre los metales) en 1556. En su obra se describen los procesos complejos y muy desarrollados de minería, extracción de los metales y metalurgia de la época. Aborda el tema eliminando el misticismo que tenía asociado anteriormente, creando una base práctica que otros podrían desarrollar. La obra describe los muchos tipos de altos hornos usados para la fundición de las menas minerales y estimuló el interés por los minerales y su composición. No es casual que mencione y use como referencia en numerosas ocasiones al autor de la antigüedad Plinio el viejo y su obra Naturalis historia . Se ha calificado a Agricola como el padre de la metalurgia.
SIGLO XIX

En el siglo xix se desarrollaron las leyes ponderales de las reacciones químicas. Para explicar estas leyes, Dalton desarrollo de la teoría atómica. Toda la química conseguida durante el siglo y medio anterior sólo tendría sentido si la materia estaba compuesta por átomos indivisibles.Enunció diferentes postulados sobre la combinación y características de los elementos. Gay-Lussac, con sus experimentos de combinación de gases, puso en tela de juicio la teoría de Dalton. Avogadrosolucionó este conflicto. Aplicó a los gases la teoría atómica y demostró que volúmenes iguales de un gas estaban formados por el mismo número de partículas. Se demostró que estas partículas estaban compuestas por grupos de átomos, llamadas “moléculas”, y no por átomos individuales. A medida que iban aumentando la lista de elementos, los químicos empezaron a verse en la necesidad de ordenarlos. Mendeleiev puso orden elaborando una “tabla periódica”.Por otra parte, Berzeliusabrió las puertas a la química orgánica; Wöler produjo la primera sustancia orgánica en el laboratorio: la Urea; Frankland descubrió los enlaces de valencia; y Kekulé
atribuyó una valencia cuatro al carbono.
Hasta el final del siglo, se desarrolló toda la teoría estructural. Otro campo que se desarrolló fue la electroquímica. Volta inventó la pila eléctrica; se estudiaron efectos de corriente eléctrica;Davy dividió diversos metales por electrolisis y Faraday
aportó las leyes cuantitativas de la electroquímica.
Finalmente, el siglo XIX vio el nacimiento de una industria química independiente, y de la profesión química.
LA QUIMICA MODERNA
Se considera a Antoine Laurent Lavoisier como el fundador de la Química Moderna. Sus aportes cubren además de la Química, múltiples áreas.
A él se le atribuye de utilizar la balanza para la demostración de las leyes fundamentales de la Química. Lavoisier demostró cuantitativamente que no era posible transformar agua en tierra, como se establecía en la teoría de los cuatro elementos. Estudio también cuidadosamente el fenómeno de la combustión y el de la calcinación. Más tarde, cuando Joseph Priestley descubrió el “aire deflogisticado”, Lavoisier comprobó que este gas se absorbía cuando los metales formaban las “cales”, y lo llamo oxígeno. Así se demostró que la teoría del flogisto era errónea.
METODO CIENTIFICO

Ciencia, es el sistema de conocimientos ordenados cuya veracidad se comprueba y se puntualiza constantemente en el curso de la práctica.
La fuerza del conocimiento científico radica en el carácter general, universal, necesario y objetivo de su veracidad. A diferencia del arte, que refleja el mundo valiéndose de imágenes artísticas, la ciencia lo aprehende en conceptos mediante los recursos del pensamiento lógico.
Frente a la religión, que ofrece una representación tergiversada y fantástica de la realidad, la ciencia formula sus conclusiones basándose en hechos.
RECURSOS METODOLOGICOS

El aporte del conocimiento metodológico compete a varias temáticas implicadas en el quehacer científico del investigador social. Los recursos en el mundo anglo son abundantes, no así en el mundo iberoamericano, aunque los españoles van muy a la zaga en estos temas. Los recursos que aquí se disponen son por tanto diversos en su origen, pero todos ellos, cual más, cual menos tienen por fin ayudar a configurar un proyecto de investigación con el suficiente soporte para configurar una propuesta metodológicamente adecuada.
CONCEPTO DE METODO
Método es una palabra que proviene del término griego methodos (“camino” o “vía”) y que se refiere al medio utilizado para llegar a un fin. Su significado original señala el camino que conduce a un lugar.
La palabra método puede referirse a diversos conceptos.
CONCEPTO DE TECNICA

La palabra técnica proviene de téchne, un vocablo de raíz griega que se ha traducido al español como “arte” o “ciencia”. Esta noción sirve para describir a un tipo de acciones regidas por normas o un cierto protocolo que tiene el propósito de arribar a un resultado específico, tanto a nivel cientifico como tecnologia ,artistico o de cualquier otro campo. En otras palabras, una técnica es un conjunto de procedimientos reglamentados y pautas que se utiliza como medio para llegar a un cierto fin.
La técnica supone que, en situaciones similares, repetir conductas o llevar a cabo un mismo procedimiento producirán el mismo efecto. Por lo tanto, se trata de una forma de actuar ordenada que consiste en la repetición sistemática de ciertas acciones.
PASOS DE METODO CIENTIFICO

1. Observación: Observar es aplicar atentamente los sentidos a un objeto o a un fenómeno, para estudiarlos tal como se presentan en realidad, puede ser ocasional o causalmente.
2. Inducción: La acción y efecto de extraer, a partir de determinadas observaciones o experiencias particulares, el principio particular de cada una de ellas.
3. Hipótesis: Planteamiento mediante la observación siguiendo las normas establecidas por el método científico.
4. Probar la hipótesis por experimentación.
5. Demostración o refutación (antítesis) de la hipótesis.
6. Tesis o teoría científica (conclusiones).
APLICACIÓN DEL METODO CIENTIFICO

Una medición es el resultado de la acción de medir. Este verbo, con origen en el término latino metiri, se refiere a la comparación que se establece entre una cierta cantidad y su correspondiente unidad para determinar cuántas veces dicha unidad se encuentra contenida en la cantidad en cuestión.
TIPOS DE MEDICIONES

UNIDADES DE MEDIDAS Y SUS CONEXIONES
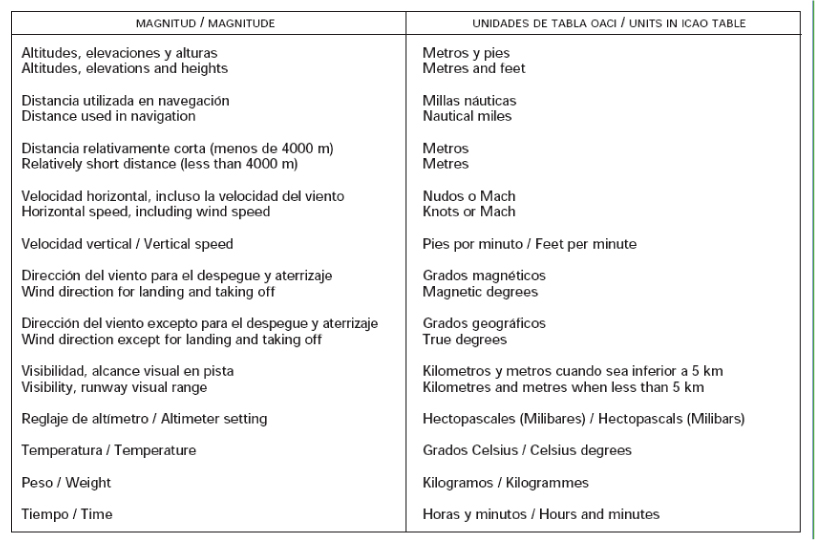
Una unidad de medida es una cantidad estandarizada de una determinada magnitud fisica , definida y adoptada por convención o por ley.Cualquier valor de una cantidad física puede expresarse como un múltiplo de la unidad de medida.
En general, una unidad de medida toma su valor a partir de un patron o de una composición de otras unidades definidas previamente. Las primeras unidades se conocen como unidades básicas o de base (fundamentales), mientras que las segundas se llaman unidades derivadas.
Un conjunto de unidades de medida en el que ninguna magnitud tenga más de una unidad asociada es denominado sistemas de unidades .
Todas las unidades denotan cantidade escalares . En el caso de las magnitud vectoriales , se interpreta que cada uno de los componentes está expresado en la unidad indicada.
POTENCIACIÓN Y NOTACION EXPONENCIAL
La potenciación es una operacion matematica entre dos términos denominados: base a y exponente n. Se escribe an y se lee usualmente como «a elevado a n» o «a elevado a la n» y el sufijo en femenino correspondiente al exponente n. Hay algunos números especiales, como el 2, al cuadrado o el 3, que le corresponde al cubo .Nótese que en el caso de la potenciación la base y el exponente pueden pertenecer a conjuntos diferentes, en unanillo totalmente general la base será un elemento del anillo pero el exponente será un numero natural que no tiene porqué pertenecer al anillo. En un cuerpo el exponente puede ser un numero entero o cero.
NOTACION EXPONENCIAL
LA MATERIA Y LA ENERGIA
LAS PROPIEDADES DE LA MATERIA
Las propiedades generales de la materia son:

CLASIFICACIÓN DE LA MATERIA
|
La materia puede clasificarse en dos categorías principales:
Las sustancias puras pueden ser elementos o compuestos, mientras que las mezclas pueden serhomogéneas o heterogéneas:
|
|
(pulsa en la figura sobre los nombres de estos 4 tipos de materia para ver sus características) |
SEPARACIÓN DE MEZCLA
, un proceso de separación se usa para transformar una mezcla de sustancias en dos o más productos distintos. Los productos separados podrían diferir en propiedades químicas o algunas propiedades físicas, tales como el tamaño o tipo de cristal.
LA ENERGIA Y LA MATERIA
|
La energía se define como la entidad intangible por medio de la cual podemos generar movimiento, trabajo y calor, la energía junto con la materia son los 2 ingredientes básicos que componen todo el universo que nos rodea. La energía es la fuente invisible que mantiene unido a los átomos y partículas subatómicas que componen toda la materia del universo, también es la fuente por medio la cual podemos aplicar movimiento a la materia, la materia es sustancia y la energía es lo que mueve a la sustancia. |
La materia es todo aquello que tiene masa y ocupa espacio. Si algo se siente pesado y ocupa un volumen entonces es materia. Pero el helio (gas) en un globo (que parece no tener masa) también es materia, sólo que flota porque el aire es más pesado (en realidad los gases también tiene masa).
TIPO DE ENERGIA
- energia electrica
- energia luminosa
- energia mecanica
- energia termica
- energia eolica
- energia solar
- energia nuclear
- energia cinetica
- energia potencial
- energia quimica
- energia hidraulica
- energia sonora
- energia radiante
- energia fotovoltaica
- energia de reaccion
- energia ionica
- energia hidroelectrica
- energia marina
- energia biovegetal
- energia libre
- energia magnetica
LEY DE LAVOISIER
TRANSFORMACIONES DE LA ENERGIA Y LA MATERIA
CONCEPTO DE ÁTOMO

Del latín atŏmum, un átomo es la cantidad menor de un elemento químico que tiene existencia propia y que está considerada como indivisible. El átomo está formado por un núcleo con protones y neutrones y por varios electrones orbitales, cuyo número varía según el elemento químico.
No obstante, además de los elementos que lo componen, es importante subrayar que todo átomo cuenta con una serie de propiedades que son fundamentales tener en cuenta a la hora de trabajar con él. En este caso, nos encontramos con el hecho de que las mismas son el tamaño, la masa, las interacciones eléctricas que se establecen entre electrones y protones o los niveles de energía.
EL ÁTOMO A TRAVÉS DEL TIEMPO
El atomismo es un sistema filosófico que surgió en Grecia durante el siglo V a. C. y en la India hacia el año 200 a. C.- 100 a. C. (Kanada), aunque tal vez mucho antes (Mosco de Sidón), según el cual el universo está constituido por combinaciones de pequeñas partículas indivisibles denominadas átomos (en griego significa que no se puede dividir).
En las antiguas creencias, el átomo se definía como el elemento más pequeño, a la vez extenso e indivisible, del que están hechas todas las cosas. Según el atomismo mecanicista deLeucipo y Demócrito (siglos V y IV a. C.), los átomos son unas partículas materiales indestructibles, desprovistas de cualidades, que no se distinguen entre sí más que por la forma y dimensión, y que por sus diversas combinaciones en el vacío constituyen los diferentes cuerpos. La concepción de la naturaleza fue absolutamente materialista, y explicó todos los fenómenos naturales en términos de número, forma y tamaño de los átomos. Incluso redujo las propiedades sensoriales de las cosas a las diferencias cuantitativas de los átomos.
ALGUNAS PROPIEDADES DEL ÁTOMO
1. Número atómico o Carga Nuclear.
2. Número de Masa, Número Másico o Peso atómico.
3. Isótopos.
4. Isóbaros.
5. Masa Atomica.
MODELO ATOMICO ACTUAL
|
Fué desarrollado durante la decada de 1920, sobre todo por Schrödinger y Heisenberg.
Es un modelo de gran complejidad matemática, tanta que usándolo sólo se puede resolver con exactitud el átomo de hidrógeno. Para resolver átomos distintos al de hidrógeno se recurre a métodos aproximados. |
MODELO DE BOHR
En 1913 Bohr publicó una explicación teórica para el espectro atómico del hidrógeno.
Basándose en las ideas previas de Max Plank, que en 1900 había elaborado una teoría sobre la discontinuidad de la energía (Teoría de los cuantos), Bohr supuso que el átomo solo puede tener ciertos niveles de energía definidos.
MODELO DE SOMMERFIELD
El modelo atómico de Sommerfeld, es otro de los modelos atómicos conocidos, este fue creado por el físico Arnold Sommerfeld de nacionalidad alemanda, quién naciera en el año 1868 y falleciera en 1951. El físico y su teoria toman como referencia básicamente la generalización relativista que posee el modelo atómico de Bohr ( modelo creado en el año 1913).
HACIA UN MODELO MECANICO-CUANTICO DE LA MATERIA
La mecánica cuántica (también conocida como la física cuántica o la teoría cuántica) es una rama de la fisica que se ocupa de los fenómenos físicos a escalas microscópicas, donde la acción es del orden de la constante de plank .Su aplicación ha hecho posible el descubrimiento y desarrollo de muchas tecnologías, como por ejemplo los transistores, componentes ampliamente utilizados en casi todos los aparatos que tengan alguna parte funcional electronica .
LA ARQUITECTURA ELECTRONICA
indica la manera en la cual los electrones se estructuran o se modifican en un átomo de acuerdo con el modelo de capas electronicas , en el cuál las funciones de ondas del sistema se expresa como un producto de orbitales
anrimetrizada .La configuración electrónica es importante porque determina las propiedades de combinación química de los átomos y por tanto su posición en la tabla periódica.
DIFERENCIA ENTRE ATOMO COMPUESTO ELEMENTO MEZCLA
El elemento es la materia descompuesta en lo mas sencillo posible.
Atomo = Sustancia pura
Los compuestos: Compuesto químico, sustancia formada por dos o más elementos que se combinan en proporción invariable. El agua, formada por hidrógeno y oxígeno, y la sal, formada por cloro y sodio, son ejemplos de compuestos químicos comunes. Tanto los elementos como los compuestos son sustancias puras.
*Características de los compuestos:
-Las partes que lo forman no pierden sus propiedades originales.
- Durante su formación no hay transformaciones de energía, la proporción de los componentes es variable.
- Sus componentes sepueden separar por medios físicos.
Las mezclas: En química, una mezcla es una combinación de dos o más sustancias en tal forma que no ocurre una reacción química y cada sustancia mantiene su identidad y propiedades. Una mezcla puede ser usualmente separada a sus componentes originales por medios físicos: destilación, disolución, separación magnética, flotación, filtración, decantación o centrifugación
*Características de las mezclas:
-Las partes que los forman pierden sus propiedades originales.
- Durante su formación no hay manifestaciones de la materia.
